全面腐食と局部腐食の違いを解説します
こんにちは。ねこぜです。
腐食形態の最も簡単な分け方の一つに、全面腐食と局部腐食で分類する方法があります。
今回は全面腐食と局部腐食の解説をします。
1.腐食は電気化学的反応
まず、鉄鋼材料に水(中性)がくっついた時に発生する腐食反応の説明をします。
全面腐食と局部腐食の違いを理解するためには、前提として反応の話が必要です。
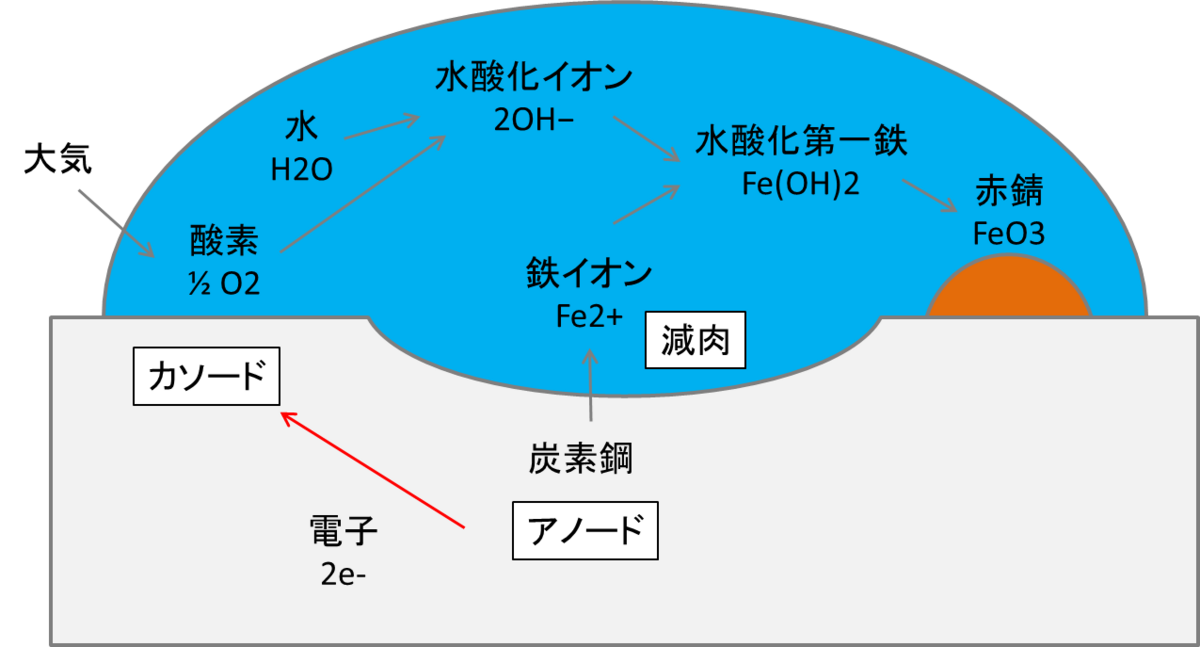
アノード側(電位が高いところ)では鉄イオンが水中に溶けて出ていきます。
つまりアノードになっている部分が減肉します。
①アノード反応:Fe → Fe2+ + 2 e−
カソード側(電位が低いところ)では水と酸素が反応して水酸化イオンが生じます。
②カソード反応:H2O + 1/2 O2 + 2e− → 2 OH−
そして鉄イオンと水酸化イオンから錆ができます。
ちなみに Fe(OH)2(水酸化第一鉄)の状態は不安定なので、FeO3(赤錆)になって錆び層を作ります。
③Fe2+ + 2 OH− → Fe(OH)2
これが腐食(湿食)の基本で、一連の反応を腐食電池といいます。
2.全面腐食
全面腐食は板厚方向に対して一様に減肉する腐食する形態のことです。
均一腐食ともいいます。
断面のイメージはこんな感じ。

全面腐食が均一に減肉する理由は、腐食電池がランダムに至るところで形成されていて、アノード位置がどんどん移動していくからです。

言い換えると、小さい腐食電池がいっぱいできて、ちょっと減肉したら減肉する位置が変わって…を繰り返している状況です。
これをミクロセル腐食といいます。
化学プラントの設備管理において、全面腐食はあまり問題になりません。
なぜかと言うと余寿命予測をしやすいからです。
減肉の程度がおおよそ均一なので肉厚の測定点を決めやすいし、腐食速度は高くても0.1mm/y以下ぐらいです。
3.局部腐食
局部腐食は減肉している箇所と健全なままの箇所の境界がはっきりしている腐食です。
断面のイメージはこれ。

局部腐食は腐食電池が固定されて反応が進みます。
この固定されている状況のことをマクロセル腐食といいます。
腐食電池が固定される理由は様々ですが、その理由によって名前(異種金属接触腐食、堆積物下腐食、隙間腐食etc.)が付く場合もあります。
腐食速度も全面腐食と比較して高く、1.0mm/yとかも普通にありえます。
化学プラントの設備管理は、局部腐食との戦いと言っても過言ではありません。
4.注意点
教科書的回答は上記なのですが、現実の化学プラントでは全面腐食と局部腐食が複合して発生していることもあります。
この設備の減肉は全面腐食だから大丈夫と思っていると、一部では局所腐食が進行している例も少なくありません。
十分な検査を行って減肉状況を把握しましょう。
5.まとめ
- 腐食は電気化学的反応(電池作用)である
- 全面腐食は腐食電池が移動する
- 局部腐食は腐食電池が固定されている
- 実機では全面腐食と局部腐食は併発するので注意
いかがだったでしょうか。
全面腐食と局部腐食は言葉の通りなので「知ってるよ」という方も多いでしょうが、意外と理解があいまいな人を見かけます。
今回の記事を読んでくださった方に新たな気づきがあると嬉しいです。